영양학또의 떠먹여주는 식품정보
[식품기사필답] 크로마토그래피의 모든것(종류,이동상고정상,HPLC등) 본문
■ 크로마토그래피
1.정의&원리
크로마토그래피(chromatography)란 다공성 흡착제 입자를 일정한 길이 만큼 충전시킨 관(column)에 용질이 들어 있는 혼합물을 통과시켜 흡착제 입자에 대한 용질의 흡착특성 차이 또는 친화성(affinity)에 근거하여 분리하는 방법이다.
=> 시간이 지나면서 흡착제에 잘 흡착되지 않는 용질은 관의 멀리까지 이동하고,
쉽게 흡착되는 용질은 이동하는 속도가 느리다.
2.이동상과 고정상
크로마토그래피 공정은 이동상(mobile phase)과 고정상(stationary phase)으로 이루어진다.
상(phase): 어떤 물질이 모든 부분에 걸쳐서 물리적 화학적으로 서로 동일한 성질을 나타낼때 표현
1) 고정상(stationary phase): 정지해 있는 균일한 성질을 가진 고체나 점성액체
ex) 흡착제, 이온교환수지, 다공성 물질, 또는 겔 등
2) 이동상(mobile phase): 균일한 하나의 상으로 이루어진 흐를 수 있는 액체,기체
<이동상의 종류>
가스 크로마토그래피 (gas chromatography, GC)
- 고감도 / 빠르다 / 간편 그러나 주입 기체 압력 조절을 잘 해야한다
- 열적으로(thermally) 안정된 휘발성 물질에 대한 분리능이 높다.
- 비휘발성 물질의 분석에는 직접 적용할 수 없다. => 생성물을 분리정제 하는데는 유용하지 않다.
- 장치: 가스도입부 - 시료주입부(injector) - column - 검출기(detector) - 기록장치

액체 크로마토그래피 (LC)
- 적당한 용매에 용해되는 비휘발성 물질의 분석에 적합
- 다성분 혼합시료의 분리와 분석에 특히 유용
3.액체크로마토그래피(LC) 종류
1) 고압액체 크로마토그래피(high-pressure liquid chromatography, HPLC)
일반적인 크로마토그래피와 같은 원리에 기초하는데, 충전관에 가해지는 높은 액체압력만 다르다.
고압의 액체와 조밀한 관충전 때문에 HPLC는 용질분자에 분리능이 높고(여러 혼합물질을 각각의 성분으로 잘 분리한다), 분리가 빠르다.

Normal phase: 고정상-극성 / 이동상-비극성 => '소수성 이동상' 먼저용출
Reverse phase(역상): 고정상-비극성 / 이동상-극성 => '친수성 이동상' 먼저용출
=> 여기서 분배계수K 개념 등장! 서로 혼합되기 어려운 두 용매에 녹는 물질의 농도비율
* 분배계수가 크다: 시료가 고정상과 친화력이 있어 천천히 용리된다.
분배계수가 작다: 시료가 고정상과 친화력이 없어 빨리 용리된다.
*용리되다: 크로마토그래피법에서 시료 중의 성분이 분리되어 뽑아내지다.
HPLC사용 범위
- 의약품의 유용물질 함량 확인
- Drug, Peptides, Protein, Vitamin, 유기합성물, 방부제, 감미료 등의 검출
- Carbamate, PAH, Vitamin E, Riboflavin 등의 검출
- 혈중에 존재하는 약물의 정성 및 정량 분석
- 시료 중에 포함된 미지 물질의 순도 검사
2) 이온교환 크로마토그래피(ion-exchange chromatography)
이온 또는 전기적으로 전하를 띠는 화합물이 정전기적인 힘에 의해 이온교환수지에 흡착되어 평형을 이루는 것에 기초한다. => 단백질 분리에 많이 사용

이온교환 크로마토그래피의 중요한 응용은 분석적인 분리에서 찾을 수 있다. 앞에서 설명한 단백질이나 아미노산의 분리는 분석적인 응용의 대표적인 예이다. 이 크로마토그래피는 양이온 및 음이온의 분리에도 효율적을 이용된다. 할로겐화물 이온은 Dowex-2 컬럼으로 pH 10.4의 1 M NaNO3 (NaOH로 조절)을 용리액으로 사용하면 F - , Cl- , Br - , I-의 순으로 분리된다. 알칼리 금속이온은 Dowex-50이나 Amberlite IR 120 컬럼으로 0.7 M HCl에 의해서 Li+ , Na + , K +의 순으 로 분리된다. 알칼리 토금속이온은 Dowex-50 컬럼에서 1.2 M 젖산암모늄에 의해서 Ca 2+, Sr 2+, Ba 2+의 순으로 용리시킬 수 있다.
3) 친화성 크로마토그래피(affinity chromatography)
용질분자와 지지체 위에 결합되어 있는 리간드(ligand) 사이의 특이한 화학적 상호작용에 기초한다.
리간드와 용질 사이의 친화성 결합은 특이적 (specific)이다.
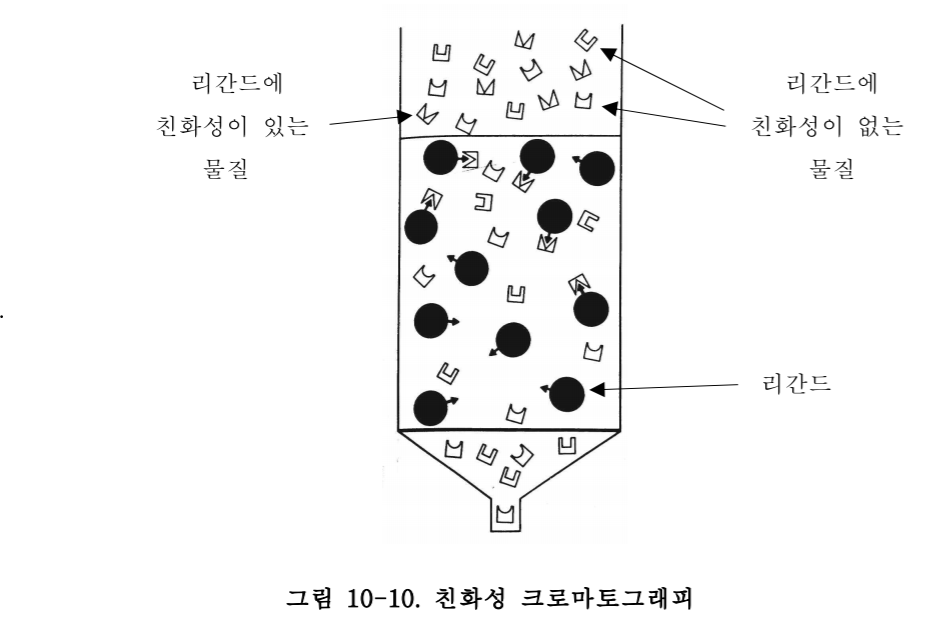
컬럼 내 정지상에 단지 한 용질과만 고유하게 상호 작용하는 리간드를 공유결합으로 붙인다. 시료를 이 컬럼에 통과시키면 단지 한 용질만 정지상에 붙게 된다.
예를 들면, 공유결합된 리간드가 특정한 단백질에 대해 항체인 경우이다. 여러 종류의 단백질을 포함한 혼합물이 컬럼을 통과할 때, 단지 항체와 반응하는 하나의 단백질만 컬럼에 결합된다. 다른 모든 단백질이 컬럼을 통해 씻겨 나간 후, pH를 변화시키거나 이온세기를 변화시킴으로써 결합되어 있는 특정한 단백질을 항체로부터 떨어지게하여 회수한다.
이러한 방법은 효소, 항원, 특이적 핵산, 비타민 결합 단백질, 약, 호르몬 수용체 같은 물질을 순수 분리할 때 자주 이용된다
친화성 크로마토그래피에서 리간드와 단백질 사이의 친화성이 너무 높거나 낮으면 좋지 않다. 기질이 리간드로 쓰일 경우에는 효소가 촉매 역할을 하지 않도록 촉매작용에 필요한 금속 이온 을 제거하거나, km과 kcat 또는 pH가 다른 경우 온도를 낮추거나 pH를 변화시킨다.
4) 겔 여과 크로마토그래피(gel filtration chromatography)
용질분자의 크기와 모양에 따른 체류시간의 차이를 이용한다. 즉, 충전입자 (packing particles) 내의 미세한 구멍으로 용질분자가 침투하여 긴 기간 동안 고체와 접촉하는 작은 입자와 구멍에 들어가지 못하여 고 체와 짧은 시간만 접촉하는 큰 분자를 분리한다.

시료분자의 크기가 팽윤된 겔의 최대 구멍(pore)보다 크면 그 분자는 겔 입자를 통과하지 못하므로 정지상 입자 사이의 공간을 통하여 비교적 빨리 관 밖으로 나온다.
구멍보다 작은 분자는 그 크기와 모양에 따라 겔 입자내의 미세한 구멍 속을 각기 다른 속도로 통과한다. 그러므로 가장 큰 분자가 먼저 관 밖으로 나오고 가장 작은 분자가 마지막에 나타난다.
5) 기타 크로마토그래피
흡착 크로마토그래피(adsorption chromatography)
액-액 분배 크로마토그래피 (liquid liquid partition chromatography)
소수성 상호반응 크로마토그래피(hydrophobic interaction chromatography)
종이 크로마토그래피 (paper chromatography)
얇은 막 크로마토그래피(thin layer chromato graphy,TLC)




'자격증 취득하자! > 식품기사' 카테고리의 다른 글
| [식품기사필답] 뉴턴유체와 비뉴턴 유체의 특성과 이용 (0) | 2020.09.21 |
|---|---|
| 식품산업에서 막 분리 공정의 원리와 개념(역삼투,한외여과,미세여과) (0) | 2020.09.17 |
| [식품기사필답]식품공전 모음8_대장균시험법(2020최신판) (0) | 2020.09.16 |
| [식품기사필답]식품공전 모음7_정성시험,정량시험,대장균군(2020최신판) (0) | 2020.09.16 |
| [식품기사필답]식품공전 모음6_일반세균수,총균수,집락수 등(2020년최신판) (0) | 2020.09.16 |




